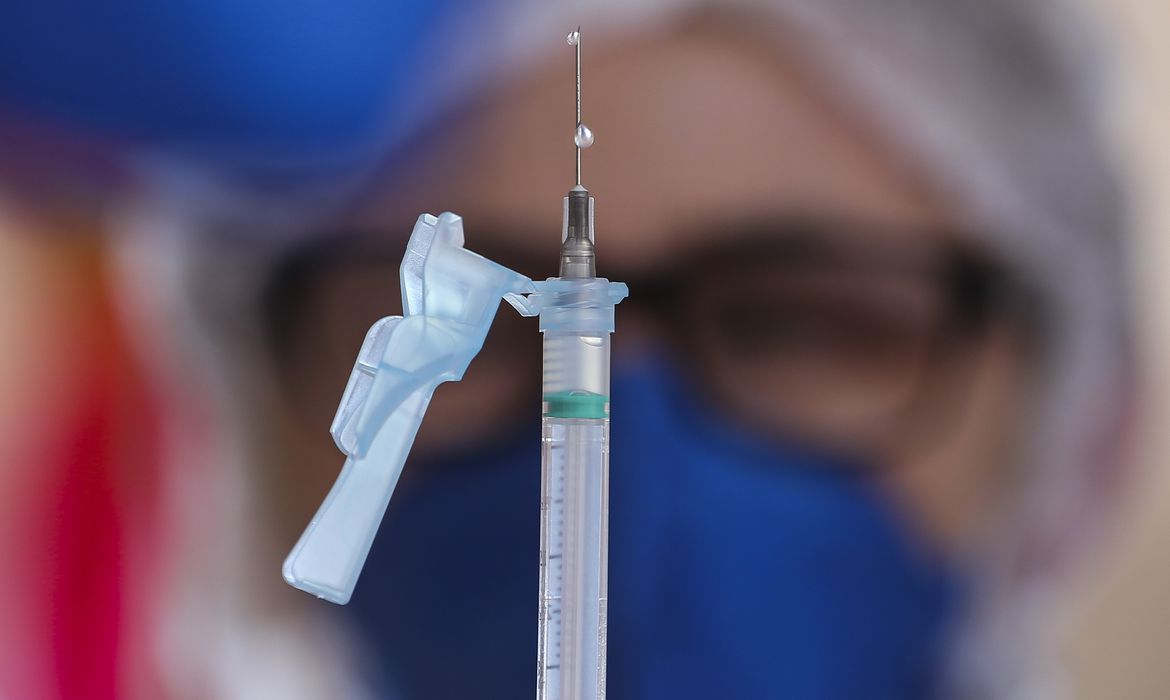
Na última segunda-feira (12), a Agência Nacional de Vigilância Sanitária (Anvisa), solicitou a alteração da bula da vacina contra Covid-19 registrada pela empresa Janssen-Cilag Farmacêutica Ltda. A alteração pede para que sejam inclusos eventos adversos que foram identificados durante a fiscalização de farmacovigilância do uso da vacina.
As novas informações de segurança incluem os seguintes eventos adversos, que também já foram relatados em notificações à Anvisa: linfadenopatia (aumento do tamanho e/ou número de linfonodos, como o aparecimento de caroços no pescoço), parestesia (sensação de dormência em alguma parte do corpo), hipoestesia (diminuição da sensibilidade da pele), tinido (zumbido no ouvido), e também diarreia e vômitos.
O prazo que empresa tem é de até 30 dias para incluir as informações na bula distribuída no Brasil.
Novos eventos adversos
Conforme o passar do tempo de comercialização e uso de qualquer medicamento no mundo inteiro, incluindo as vacinas, novos eventos adversos tem risco de acontecer.
Por esse motivo que existe a farmacovigilância, que acompanha e avalia sistematicamente o perfil benefício-risco das vacinas.
Porém, conforme a Anvisa, até o momento, os benefícios de todas as vacinas aprovadas pela agência superam seus riscos.
Receba as notícias do OCP no seu aplicativo de mensagens favorito:
- Grupo de Blumenau e região
- Grupo de Criciúma e região
- Grupo de Florianópolis
- Grupo de Jaraguá do Sul
- Grupo de Joinville